
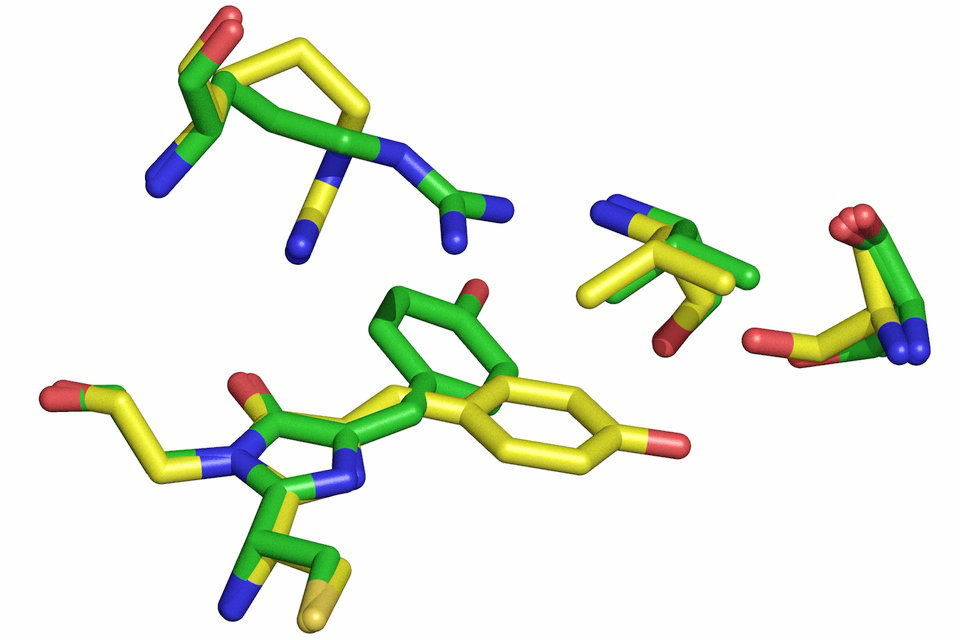
एक क्रोमोफोर उसके रंग के लिए जिम्मेदार एक अणु का हिस्सा है। हमारी आँखों से जो रंग देखा जाता है, वह दृश्य प्रकाश के एक निश्चित तरंगदैर्ध्य स्पेक्ट्रम के भीतर अवशोषित नहीं होता है। क्रोमोफोर अणु में एक क्षेत्र है जहां दो अलग आणविक ऑर्बिटल्स के बीच ऊर्जा अंतर दृश्यमान स्पेक्ट्रम की सीमा के भीतर आता है। क्रोमोफोर को मारने वाले दर्शनीय प्रकाश को इस तरह से एक उत्साहित राज्य में रोमांचक एक इलेक्ट्रॉन द्वारा भूजल राज्य से अवशोषित किया जा सकता है।
जैविक अणुओं में जो प्रकाश ऊर्जा को पकड़ने या पहचानने के लिए काम करते हैं, क्रोमोफोर, आकृति है, जो प्रकाश से आते समय परमाणु के गठनात्मक परिवर्तन का कारण बनता है।
संयुग्मित पी-बॉन्ड सिस्टम क्रोमोफोर्स
संयुग्म क्रोमोफोर्स में, एकमात्र वैकल्पिक और डबल बांड की एक श्रृंखला द्वारा बनाई गई ऊर्जा स्तरों के बीच इलेक्ट्रोन कूदता है, जिसे पीआई ऑर्बिटल्स बढ़ाया जाता है, जो अक्सर सुगन्धित तंत्र में होता है। सामान्य उदाहरणों में रेटिना (प्रकाश का पता लगाने के लिए आंखों में प्रयोग किया जाता है), विभिन्न खाद्य रंग, कपड़े के रंग (एज़ो संयुग्म), पीएच संकेतक, लाइकोपीन, बीओ-कैरोटीन और एंथोकायनिन शामिल हैं। क्रोमोफोर की संरचना में विभिन्न कारक क्रोमॉफ़ोर के अवशोषित स्पेक्ट्रम में क्या तरंग दैर्ध्य क्षेत्र में निर्धारित करने के लिए जाते हैं। एक अणु में अधिक असंपृक्त (बहु) बॉन्ड के साथ एक संयुग्मित प्रणाली को बढ़ाते हुए या बढ़ाते हुए लंबे समय तक तरंग दैर्ध्य में अवशोषण में बदलाव लाएंगे। वुडवर्ड-फाइसर नियमों का इस्तेमाल संयुग्मित पीआई-बॉन्ड सिस्टम के साथ कार्बनिक यौगिकों में अनुमानित पराबैंगनी-दृश्य अधिकतम अवशोषण तरंग दैर्ध्य के लिए किया जा सकता है।
इनमें से कुछ धातु कॉम्प्लेक्स क्रोमोफोर्स हैं, जिसमें लगीड्स के साथ समन्वय परिसर में एक धातु होती है। उदाहरण क्लोरोफिल हैं, जिसका उपयोग प्रकाश संश्लेषण और हीमोग्लोबिन के पौधों द्वारा किया जाता है, जो कशेरुक जानवरों के रक्त में ऑक्सीजन ट्रांसपोर्टर होता है। इन दो उदाहरणों में, एक धातु टेट्रापायरोलल मैक्रोसायकल की अंगूठी के केंद्र में जटिल हो जाती है: क्लोरोफिल के मामले में क्लोरीन-प्रकार की अंगूठी में हीमोग्लोबिन या मैग्नीशियम कॉम्प्लेक्स के हेम समूह (लौह को पोर्फिरिन अंगूठी में लोहे) में लोहे होता है। । मैक्रोसाइटिकल रिंग की अत्यधिक संयुग्मित पी-बॉन्डिंग सिस्टम दृश्य प्रकाश को अवशोषित करती है। केंद्रीय धातु की प्रकृति धातु-मैक्रोकसील परिसर के अवशोषण स्पेक्ट्रम या उत्तेजित राज्य जीवनकाल जैसे गुणों को भी प्रभावित कर सकती है। कार्बनिक यौगिकों में टेट्रापीरॉल मूवमेंट जो मैक्रोोजेक्लिक नहीं है लेकिन फिर भी संयुग्मित पीआई-बॉन्ड सिस्टम अभी भी क्रोमोफोर के रूप में कार्य करता है। ऐसे यौगिकों के उदाहरण में बिलीरुबिन और यूरोबिलिन शामिल हैं, जो एक पीले रंग का रंग दिखाते हैं।
Auxochrome
एक ऑक्सोक्रोम क्रोमोफोर से जुड़े परमाणुओं के एक कार्यात्मक समूह है जो प्रकाश को अवशोषित करने के लिए क्रोमोफोर की क्षमता को संशोधित करता है, तरंग दैर्ध्य या अवशोषण की तीव्रता को बदलता है।
क्रोमोफोर्स में हालोक्रोमिक्स
Halochromism तब होता है जब एक पदार्थ पीएच परिवर्तन के रूप में रंग बदलता है यह पीएच संकेतकों की एक संपत्ति है, जिसका आणविक संरचना आसपास के पीएच में कुछ बदलावों पर बदलाव करता है। संरचना में यह परिवर्तन पीएच संकेतक अणु में क्रोमोफोर को प्रभावित करता है। उदाहरण के लिए, phenolphthalein एक पीएच संकेतक है जिसका संरचना पीएच परिवर्तन के रूप में बदलता है जैसा कि निम्न तालिका में दिखाया गया है:
| Structure | ||
|---|---|---|
| pH | 0-8.2 | 8.2-12 |
| Conditions | acidic or near-neutral | basic |
| Color name | colorless | pink to fuchsia |
| Color |
लगभग 0-8 की एक पीएच श्रेणी में, अणु के तीन सुगंधित रिंग हैं, जो सभी बंधे हुए हैं, जो टेट्राहेड्रल स्पीड 3 हाइब्रिज्ड कार्बन परमाणु के मध्य में होते हैं जो खुशबूदार छल्ले संयुग्मित में π-बंधन नहीं बनाते। उनके सीमित हद तक, सुगंधित रिंग केवल पराबैंगनी क्षेत्र में प्रकाश को अवशोषित करते हैं, और इसलिए यौगिक 0-8 पीएच श्रेणी में रंगहीन दिखाई देता है। हालांकि, जैसा कि पीएच 8.2 से आगे बढ़ता है, केंद्रीय केंद्रीय कार्बन एक डबल बांड का हिस्सा बन जाता है जिससे एसपी 2 हाइब्रिज्ड हो जाता है और रिंगों में π-bonding के साथ ओवरलैप करने के लिए पी ऑर्बिटल को छोड़ देता है। इससे तीन रिंग एक साथ फैजासीया रंग दिखाने के लिए लंबे समय तक तरंगदैर्ध्य दृश्य प्रकाश को अवशोषित करने के लिए विस्तारित क्रोमोफोर बनाने के लिए एक साथ मिलते हैं। 0-12 से बाहर पीएच पर्वतमाला पर, अन्य आणविक संरचना परिवर्तन का परिणाम अन्य रंग परिवर्तनों में होता है; विवरण के लिए फ़िनोल्फाथेलिन देखें